Inhaltsverzeichnis
Produktbeschreibung
Gebrauchsinformation
Bezeichnung des Tierarzneimittels
Profender 15 mg/3 mg Tabletten mit veränderter Wirkstofffreisetzung für kleine Hunde
Profender 50 mg/10 mg Tabletten mit veränderter Wirkstofffreisetzung für mittelgroße Hunde
Profender 150 mg/30 mg Tabletten mit veränderter Wirkstofffreisetzung für große Hunde
Anwendungsgebiete
Für Hunde, bei denen eine parasitäre Mischinfektion vorliegt oder das Risiko einer parasitären Mischinfektion durch Rund- und Bandwürmer der folgenden Arten besteht:
Rundwürmer (Nematoden)
Toxocara canis (unreife und reife adulte Stadien, L4 und L3)
Toxascaris leonina (unreife und reife adulte Stadien, L4)
Ancylostoma caninum (unreife und reife adulte Stadien)
Uncinaria stenocephala (unreife und reife adulte Stadien)
Trichuris vulpis (unreife und reife adulte Stadien, L4)
Bandwürmer (Cestoden)
Dipylidium caninum
Taenia spp.
Echinococcus multilocularis (reife adulte und unreife Stadien)
Echinococcus granulosus (reife adulte und unreife Stadien)
Zieltierarten
Hund
Genehmigungsdatum der Packungsbeilage
Januar 2021
Detaillierte Angaben zu diesem Tierarzneimittel finden Sie auf der Website der Europäischen Arzneimittel-Agentur unter http://www.ema.europa.eu/
Weitere Angaben
Packungsgrößen:
Profender 15 mg/3 mg Tabletten mit veränderter Wirkstofffreisetzung für kleine Hunde
- 2 Tabletten (1 Blisterstreifen)
- 4 Tabletten (1 Blisterstreifen)
- 10 Tabletten (1 Blisterstreifen)
- 24 Tabletten (3 Blisterstreifen mit jeweils 8 Tabletten)
- 50 Tabletten (5 Blisterstreifen mit jeweils 10 Tabletten)
Profender 50 mg/10 mg Tabletten mit veränderter Wirkstofffreisetzung für mittelgroße Hunde
- 2 Tabletten (1 Blisterstreifen)
- 4 Tabletten (1 Blisterstreifen)
- 6 Tabletten (1 Blisterstreifen)
- 24 Tabletten (4 Blisterstreifen mit jeweils 6 Tabletten)
- 102 Tabletten (17 Blisterstreifen mit jeweils 6 Tabletten)
Profender 150 mg/30 mg Tabletten mit veränderter Wirkstofffreisetzung für große Hunde
- 2 Tabletten (1 Blisterstreifen)
- 4 Tabletten (1 Blisterstreifen)
- 24 Tabletten (6 Blisterstreifen mit jeweils 4 Tabletten)
- 52 Tabletten (13 Blisterstreifen mit jeweils 4 Tabletten)
Es werden möglicherweise nicht alle Packungsgrößen in Verkehr gebracht.
Verschreibungspflichtig
Zusammensetzung
Wirkstoff(e) und sonstige Bestandteile:
Jede Profender-Tablette enthält:
| Emodepsid | Praziquantel | |
| Profender Tabletten für kleine Hunde | 3 mg | 15 mg |
| Profender Tabletten für mittelgroße Hunde | 10 mg | 50 mg |
| Profender Tabletten für große Hunde | 30 mg | 150 mg |
Gegenanzeigen
Nicht anwenden bei Hundewelpen, die jünger als 12 Wochen oder leichter als 1 kg sind.
Nicht anwenden bei bekannter Überempfindlichkeit gegenüber den Wirkstoffen, oder einem der sonstigen Bestandteile.
Nebenwirkungen
Vorübergehende leichte Magen-Darm-Störungen (wie Speicheln, Erbrechen) wurden in sehr seltenen Fällen beobachtet. Vorübergehende leichte neurologische Störungen (wie Zittern, Koordinationsstörungen) wurden in sehr seltenen Fällen beobachtet. Der erforderliche Futterentzug scheint in diesen Fällen nicht beachtet worden zu sein. Darüber hinaus können bei Collies, Shelties und Australian Shepherds mit MDR-1-Gendefekt [MDR-1-(-/-)] die Anzeichen neurologischer Störungen (z. B. Konvulsionen) schwerer sein. Spezifische Gegenmittel sind nicht bekannt.
Die Angaben zur Häufigkeit von Nebenwirkungen sind folgendermaßen definiert:
- Sehr häufig (mehr als 1 von 10 behandelten Tieren zeigen Nebenwirkungen)
- Häufig (mehr als 1 aber weniger als 10 von 100 behandelten Tieren)
- Gelegentlich (mehr als 1 aber weniger als 10 von 1000 behandelten Tieren)
- Selten (mehr als 1 aber weniger als 10 von 10.000 behandelten Tieren)
- Sehr selten (weniger als 1 von 10.000 behandelten Tieren, einschließlich Einzelfallberichte).
Falls Sie Nebenwirkungen, insbesondere solche, die nicht in der Packungsbeilage aufgeführt sind, bei Ihrem Tier feststellen, oder falls Sie vermuten, dass ein Tierarzneimittel nicht gewirkt hat, teilen Sie dies bitte Ihrem Tierarzt oder Apotheker mit.
Anwendung
Dosierung für jede Tierart, Art und Dauer der Anwendung
Zum Eingeben bei Hunden, die älter als 12 Wochen und mindestens 1 kg schwer sind.
Profender wird mit einer Mindestdosis von 1 mg Emodepsid / kg Körpergewicht und 5 mg Praziquantel / kg Körpergewicht entsprechend der folgenden Dosierungstabelle verabreicht.
Pro Behandlung ist eine einmalige Anwendung ausreichend.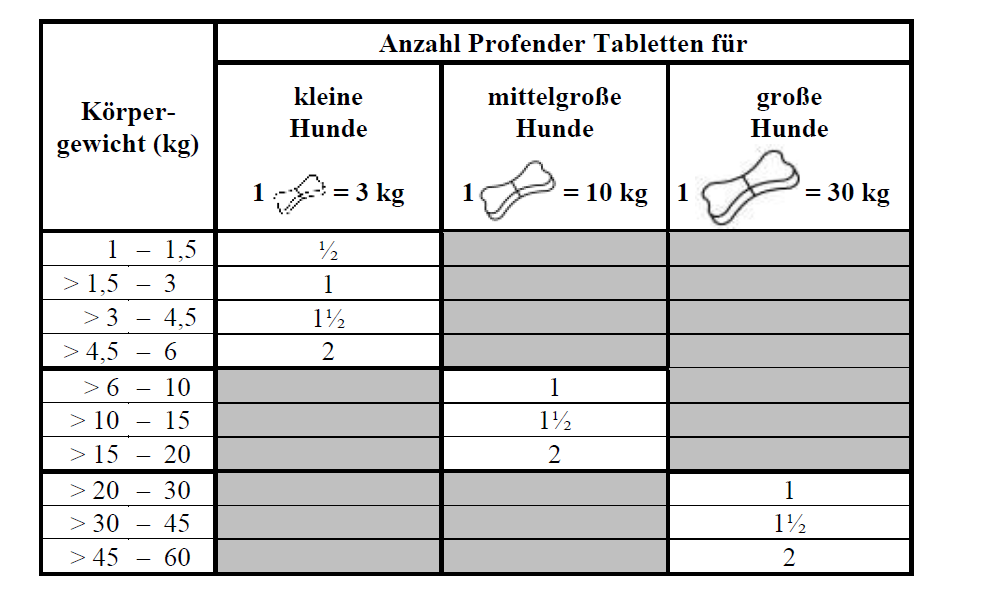
Hinweise für die richtige Anwendung
Profender Tabletten sind mit Fleisch-Geschmackstoffen versetzt und werden von Hunden normalerweise ohne zusätzliches Futter gut akzeptiert. Nur bei nüchternen Tieren anwenden. Zum Bespiel wird empfohlen, den Hund über Nacht fasten lassen, wenn die Behandlung am Morgen stattfindet. Nach der Behandlung darf dem Hund vier Stunden lang kein Futter gegeben werden.
Wartezeit
Nicht zutreffend.
Besondere Lagerungshinweise
Arzneimittel unzugänglich für Kinder aufbewahren.
In der Originalverpackung aufbewahren, um den Inhalt vor Feuchtigkeit zu schützen.
Sie dürfen das Arzneimittel nach dem auf dem Etikett und dem Karton angegebenen Verfalldatum nicht mehr verwenden. Das Verfalldatum bezieht sich auf den letzten Tag des Monats.
Besondere Warnhinweise
Besondere Warnhinweise für jede Zieltierart
Besondere Warnhinweise für jede Zieltierart
Nach häufiger, wiederholter Anwendung von Wirkstoffen derselben Substanzklasse von Anthelminthika kann sich eine Resistenz gegen diese Substanzklasse entwickeln.
Besondere Vorsichtsmaßnahmen für die Anwendung bei Tieren
Nur bei nüchternen Tieren anwenden. Zum Bespiel wird empfohlen, den Hund über Nacht fasten lassen, wenn die Behandlung am Morgen stattfindet. Nach der Behandlung darf dem Hund vier Stunden lang kein Futter gegeben werden.
Bei Vorliegen einer Infektion mit Dipylidium caninum wird eine begleitende Behandlung gegen Zwischenwirte wie Flöhe und Haarlinge empfohlen, um einer Reinfektion vorzubeugen.
Es wurden keine Studien mit stark geschwächten Tieren oder Tieren mit stark eingeschränkter Leber- oder Nierenfunktion durchgeführt. Deshalb sollte bei diesen Tieren die Anwendung des Tierarzneimittels nur auf der Basis einer Nutzen-Risiko-Bewertung erfolgen.
Besondere Vorsichtsmaßnahmen für den Anwender
Aus hygienischen Gründen wird empfohlen, nach der Verabreichung der Tabletten die Hände zu waschen. Wenn das Tierarzneimittel versehentlich geschluckt wurde, besonders wenn Kinder betroffen sind, ist ein Arzt zu Rate zu ziehen und die Packungsbeilage oder das Etikett vorzuzeigen.
Echinokokkose stellt eine Gefahr für den Menschen dar. Da es sich bei der Echinokokkose um eine gegenüber der Weltorganisation für Tiergesundheit (OIE) meldepflichtige Erkrankung handelt, sind hinsichtlich der Behandlung, der Nachkontrollen und des Schutzes von Personen besondere Richtlinien zu beachten, die bei den zuständigen Behörden zu beziehen sind.
Anwendung während der Trächtigkeit oder Laktation
Kann während der Trächtigkeit und Laktation angewendet werden.
Wechselwirkungen mit anderen Arzneimitteln und andere Wechselwirkungen:
Emodepsid ist ein Substrat für P-Glykoprotein. Die gleichzeitige Behandlung mit anderen Tierarzneimitteln, die P-Glykoproteinsubstrate oder -inhibitoren sind (z. B. Ivermectin und andere antiparasitär wirksame makrozyklische Laktone, Erythromycin, Prednisolon und Cyclosporin) könnte pharmakokinetische Wechselwirkungen hervorrufen. Die möglichen klinischen Folgen solcher Wechselwirkungen wurden nicht untersucht.
Überdosierung (Symptome, Notfallmaßnahmen und Gegenmittel) falls erforderlich
Bei bis zu fünffacher Überdosierung wurden gelegentlich kurzzeitiges Muskelzittern, Koordinations-störungen und Trägheit beobachtet. Bei MDR1-defekten (-/-)Collies ist die therapeutische Breite im Vergleich zu anderen Hunderassen reduziert; nach Gabe der doppelten empfohlenen Dosis wurde bei Hunden, die wie vorgegeben nüchtern waren, gelegentlich kurzzeitiges, leichtes Zittern und/oder Ataxie beobachtet.
Die Symptome klingen ohne Behandlung vollständig ab. Eine Fütterung kurz vor oder kurz nach der Tabletteneingabe kann die Häufigkeit und Intensität solcher Überdosierungssymptome verstärken und gelegentlich zu Erbrechen führen. Ein spezifisches Gegenmittel ist nicht bekannt.
Inkompatibilitäten
Nicht zutreffend.
Besondere Vorsichtsmaßnahmen für die Entsorgung von nicht verwendeten Arzneimitteln oder von Abfallmaterialien, sofern erforderlich
Nicht verwendete Tierarzneimittel oder davon stammende Abfallmaterialien sind entsprechend den örtlichen Vorschriften zu entsorgen.
Nicht verbrauchte halbe Tabletten dürfen nicht für den weiteren Gebrauch gelagert werden und sollten in Übereinstimmung mit den örtlichen Vorschriften entsorgt werden.
Zulassung / Hersteller
NAME UND ANSCHRIFT DES ZULASSUNGSINHABERS UND, WENN UNTERSCHIEDLICH DES HERSTELLERS, DER FÜR DIE CHARGENFREIGABE VERANTWORTLICH IST:
Zulassungsinhaber:
Vetoquinol S.A.
Magny-Vernois
70200 Lure
Frankreich
Für die Chargenfreigabe verantwortlicher Hersteller:
KVP Pharma + Veterinär Produkte GmbH
Projensdorfer Str. 324
24106 Kiel
Deutschland

